
欧盟医疗器械法规符合性评价程序要求的技术文档
欧盟医疗器械法规符合性评价程序要求的技术文档
TÜV南德将根据客户的个人情况设计对应的评审日程。可以加快部分内容的评审,即以最高优先级处理。下图为南德基本认证服务与加急服务的比较。
请注意,快速通道服务也需在适当资源可用的情况下进行。
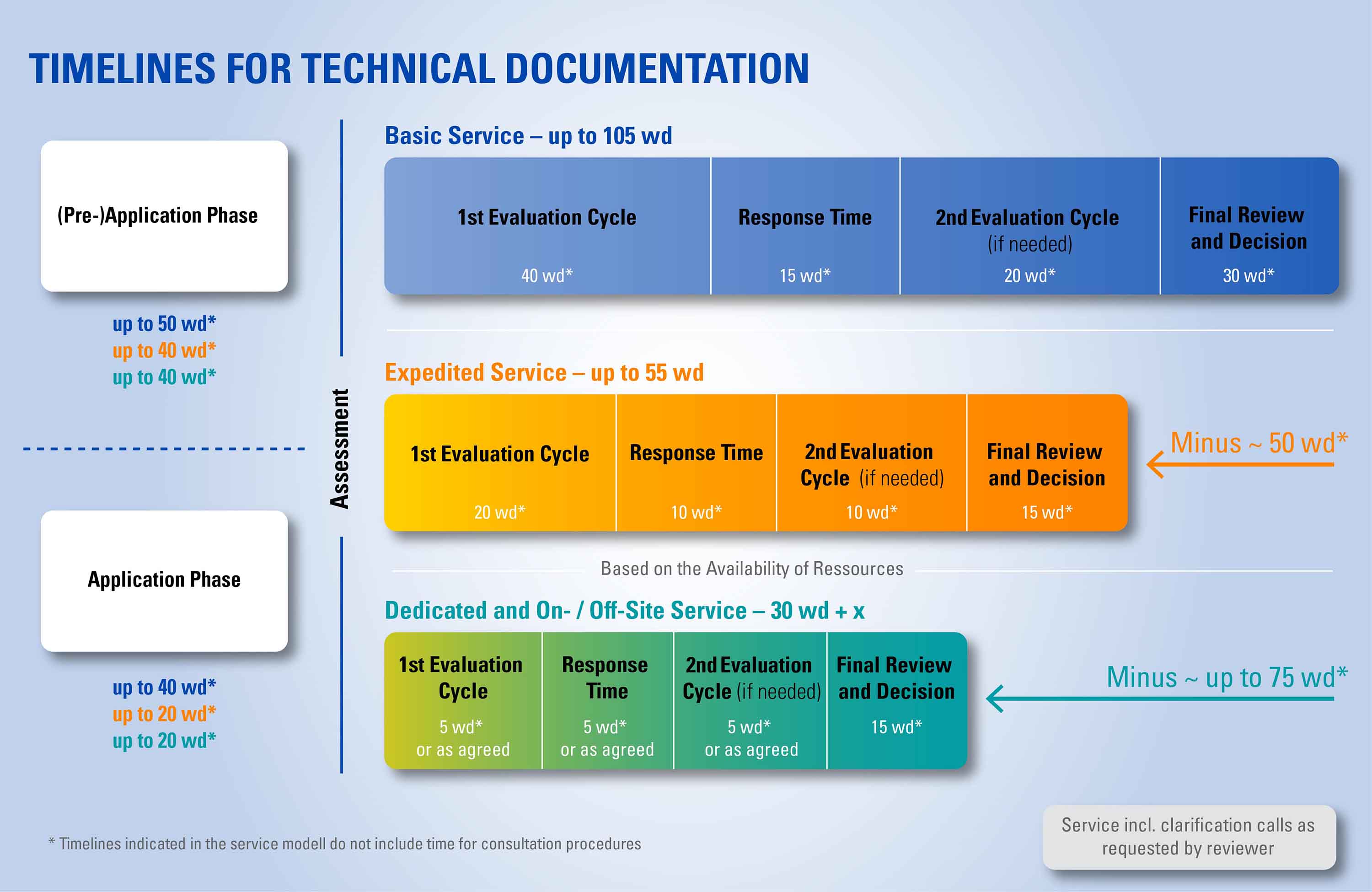
TÜV南德给出的日程为预估计划日程。各公司或个人的日程可能有所不同。在特定地区提供快速通道服务。

According to the Medical Device Regulation (EU) 2017/745 (MDR)
Download

Site Selector
Global
Asia
Europe
Middle East and Africa
