进入全球市场
TÜV南德意志集团是世界领先的技术服务公司之一,为客户提供测试、认证、检验等服务。150多年的德国卓越技术,帮助制造商将产品更快、更有效地推向市场。
New MDR 法规专题讲座
我们真诚邀请您参加于2021年07月07日至07月09日由TÜV南德意志集团医疗、健康服务部门在南京举办的New MDR法规专题讲座。
2017年5月,欧盟医疗器械新法规MDR (REGULATION EU 2017/745) 颁布,新的法规将替代原有的医疗器械指令 (MDD 93/42/EEC) 和有源植入性医疗器械指令 (AIMD 90/385/EEC)。新法规在各方职责、产品分类、符合性评估途径、临床数据等方面都做出了重大变化,提出了很多新的、更高的要求。已通过MDD指令CE认证的产品,也需要重新评估后才能获得MDR CE证书。虽然新法规给企业3年的过渡期,但实际企业有很多转换工作需要执行。此次重大变更,在欧盟医疗器械历史上具有“革命性”的意义。如何才能满足新法规的要求,已成为中国制造商面对的巨大挑战。
我们希望借助此次培训让企业在质量管理体系运行、如何按MDR进行CE认证进入欧盟市场有清晰的认识。
与会者通过考试后将获得一张由我司颁发的New MDR培训证书
培训安排

日程安排
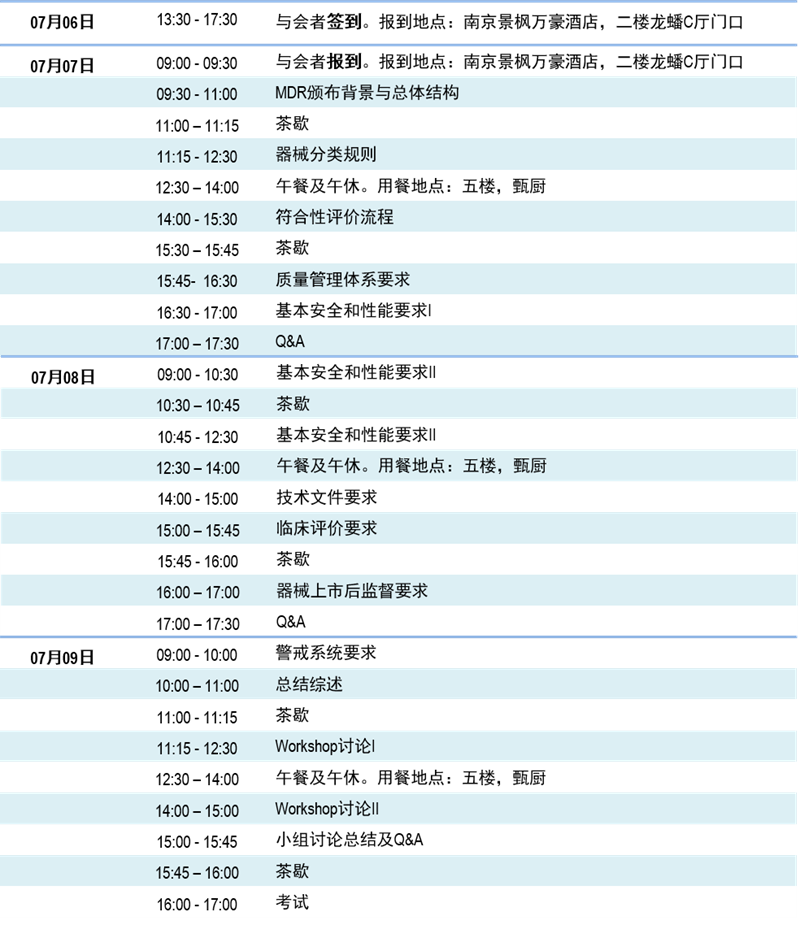
讲师介绍

报名方式
您可扫描下方二维码,即刻报名!

或直接联系:
韩蕾 女士
电话:+86 21 6141 0172/13764997561
电邮:lei.han@tuvsud.com
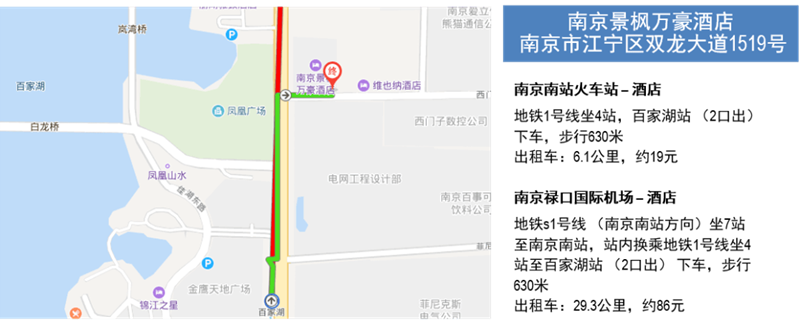
培训地址
南京景枫万豪酒店
南京市江宁区双龙大道1519号
Site Selector
Global
Asia
Europe
Middle East and Africa
